| 臨床研究名 | 進行性膠芽腫患者に対する増殖型遺伝子組換え単純ヘルペスウイルスG47Δを用いたウイルス療法の臨床研究 |
|---|---|
| 始めに | この臨床研究は、膠芽腫に対する新たな治療法の開発を目的に、東京大学医学部附属病院脳神経外科で実施します。G47Δという遺伝子組換え型単純ヘルペスウイルスを用いることから、実施計画は東京大学医学部の遺伝子治療臨床研究審査委員会に加えて、厚生労働大臣の承認を得ています。 新しい治療薬の開発は、一般に安全性を確かめるための臨床試験を行い、その後、少数の患者を対象に治療効果を調べる臨床試験、そして多数の患者を対象に治療効果や安全性を検証する臨床試験という順に実施していきます。今回の臨床研究は、その最初の段階であり、参加されても病気の回復に結びつかない可能性があります。しかし、このような臨床試験が進めば、膠芽腫に対する新しい治療法を確立するために役にたつ可能性があります。 なお、今回の臨床研究は、製薬会社などが行い、厚生労働省から医薬品としての承認を取得するための臨床試験、いわゆる「治験」ではありません。 |
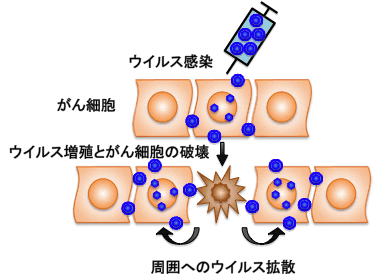
| 試験の概略 | 臨床研究の対象となるのは、膠芽腫の患者で、手術と放射線治療をすでに行い、腫瘍が再発した、もしくは腫瘍が大きくなってきている場合です。膠芽腫は脳腫瘍の一種で、現在のところ手術や放射線治療、化学療法などを組み合わせた総合的な治療が行われていますが、進行を食い止めることが困難な病気です。今回の臨床研究は、増殖するウイルスで腫瘍細胞を破壊するという全く新しい方法を試みます。 G47Δという遺伝子組換えヘルペスウイルスを定位脳手術により腫瘍内に投与します。 G47Δのもととなった単純ヘルペスウイルスI型は、口唇に水疱を生じる口唇ヘルペスの原因ウイルスですが、ごくまれに角膜炎や重症の脳炎を起こすことが知られています。単純ヘルペスウイルスI型の3つの遺伝子に組み換え技術を用いて人為的変異を加え、腫瘍細胞だけで増殖し正常組織を傷つけないように工夫したのがG47Δです。 G47Δを腫瘍に感染させると、G47Δが増殖→腫瘍細胞を破壊→増えたG47Δが周りの腫瘍細胞に感染→G47Δが増殖→腫瘍細胞を破壊、を繰り返して腫瘍を縮小させると期待されます。今回の臨床研究は、G47Δが安全かどうかを確かめることが第一の目的です。
|
| 参加のための 主な規準 |
・手術をすでに受け、病理診断で膠芽腫と診断されていること。 ・放射線治療後の腫瘍の再発あるいは放射線治療中の腫瘍増大であること。 ・再発(進行)した腫瘍はMRIで造影される1cm以上の病変で、1つだけであること。 ・介助なしに生活できる状態であること。 ・18歳以上であること。 ・他の癌を合併または過去に経験していないこと。 ・重篤な合併疾患や検査値異常のないこと。 ・1ヶ月以内に他の臨床試験薬の投与を受けていないこと。 |
| 資料 |
被験者登録は終了しました